
-

生物通官微
陪你抓住生命科技
跳动的脉搏
口腔癌细胞如何躲避免疫系统
【字体: 大 中 小 】 时间:2024年09月18日 来源:AAAS
编辑推荐:
一项新的研究发现了口腔癌用来逃避免疫系统的途径,可能为改进治疗打开了大门,包括蛋白质相互作用可能是对抗侵袭性形式的关键。
澳大利亚麦考瑞大学(Macquarie University)的研究人员发现了口腔癌细胞如何阻碍人体免疫反应的新信息。这可能会为这种侵袭性疾病带来更好的治疗方法。他们的研究发表在本月的《口腔生物科学杂志》上,研究了口腔癌细胞中的蛋白质如何相互作用可能会阻止我们的免疫细胞攻击这些肿瘤。
口腔癌包括唇癌、舌癌、颊癌、口腔癌、上颚癌、鼻窦癌和喉癌。口腔癌是澳大利亚第六大常见癌症,也是印度最常见的癌症。危险因素包括吸烟、酗酒和HPV感染。早期发现大大提高了口腔癌的存活率。然而,晚期口腔癌很难有效治疗,患者通常存活不到12个月。免疫疗法旨在增强人体对癌症的天然防御能力,它在某些癌症上显示出了希望,但在口腔癌上收效甚微。
麦考瑞大学应用生物科学的第一作者Rajdeep Chakraborty 博士说,这项研究为口腔癌如何避开免疫系统提供了重要线索:“我们认为可能是口腔癌细胞中的蛋白质共同作用减少了免疫细胞的攻击。”Chakraborty博士也是一名牙槽外科医生和麦考瑞大学博士毕业生。
抗治疗性
这项研究的重点是一种名为“转录信号传感器和激活因子3”的蛋白质,简称为STAT3,它有助于口腔癌细胞的生长。该团队使用先进的蛋白质组学技术来观察STAT3在口腔癌细胞中与哪些其他蛋白质相互作用。研究结果表明,STAT3和它的蛋白伴侣可能作为一种干扰因子,在口腔癌的抗癌治疗中掩护癌细胞使其不被靶向。
Chakraborty博士为这项研究开发了一种新的三维癌症模型,现已获得专利。“我开发的三维癌症模型将癌细胞与免疫细胞放在一起,而不是使用通常无法转化为人类研究的小鼠模型。提取和制备人类口腔组织细胞,在三维模型让免疫细胞同时与口腔癌细胞相互作用,以模拟肿瘤的行为。”然后,研究人员在3D模型上使用质谱法来识别与STAT3相互作用的蛋白质。
研究人员发现,与正常口腔细胞相比,STAT3在所有类型的口腔癌细胞中的含量都要高得多。在口腔癌细胞中,一种叫做表皮生长因子受体(EGFR)的蛋白质与STAT3密切相关,还有其他几种与STAT3相互作用的蛋白质参与控制免疫系统,包括一些已知的抑制它的蛋白质。分析表明,STAT3及其伴侣蛋白可能参与了帮助癌症避开免疫系统的途径。
研究背景:STAT3是帮助口腔鳞状细胞癌(OSCC)进展的关键增殖机制相关蛋白之一。STAT3免疫逃避是由JAK2/STAT3/PDL1信号轴介导的。基于之前的研究结果,我们假设STAT3结合伴侣参与了OSCC抗肿瘤活性的抑制。
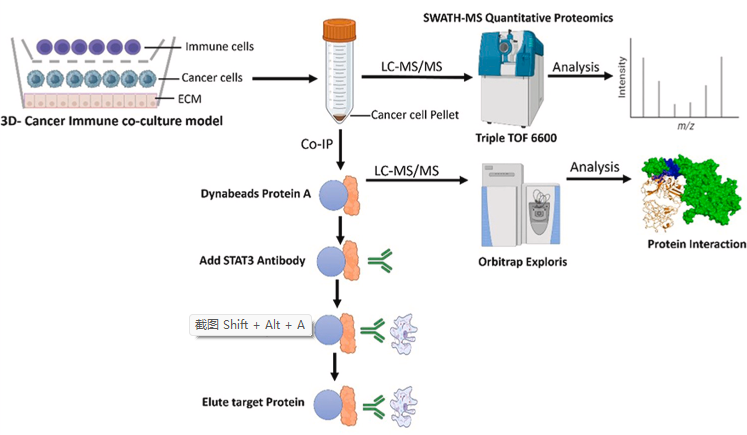
研究方法:以口腔癌细胞系SCC4、SCC9、SCC25和CAL27与正常口腔细胞系OKF6构建三维肿瘤免疫共培养模型。细胞与NK-92和Jurkat细胞共培养。根据SWATH数据选择靶蛋白STAT3,并进行基于共免疫沉淀(Co-IP)的蛋白质组学研究。对Co-IP LC-MS/MS输出进行分析,以确定蛋白质相互作用网络、基因本体、途径分析和蛋白质簇注释。
研究结果:口腔癌细胞系中的STAT3与表皮生长因子受体(EGFR)和其他参与增殖和免疫机制的蛋白相互作用。蛋白质组学分析表明,本研究中发现的一些STAT3结合蛋白是已知的免疫系统调节因子。
研究结论:总的来说,STAT3相互作用蛋白调节口腔鳞状细胞癌细胞的免疫系统。
作者视角
Chakraborty博士说,这项研究为口腔癌治疗开辟了新的可能性,特别是解决耐药性问题。该团队目前正在探索联合治疗方法,如将STAT3单克隆或工程抗体与EGFR治疗相结合。“第一阶段和第二阶段的初步报告表明这是有效的。”“这项研究揭示了潜在的新药物靶点,可以帮助增强对口腔癌细胞的免疫反应。”需要更多的研究来证实结果并开发潜在的治疗方法。“这是重要的第一步,但我们现在需要确认这些蛋白质的相互作用,看看靶向它们是否能增强抗肿瘤免疫反应。”
这一发现也可以解释为什么一些口腔癌对现有的免疫疗法产生抗药性。来自麦考瑞大学自然科学学院的Fei Liu副教授是一位对针对癌症机制的精确治疗感兴趣的化学家,也是该研究的合作者。Liu说,研究小组在这项研究中使用了一系列技术,包括3D细胞培养、蛋白质组学和生物信息学分析。“这种多管齐下的方法使研究人员能够在一个模型中检查潜在的意想不到的蛋白质相互作用,该模型可能更好地模拟真实肿瘤的环境。”
耐药性
Chakraborty博士说:“我们的初步数据可以阐明为什么侵袭性口腔癌经常对西妥昔单抗产生耐药性,西妥昔单抗是FDA批准的主要靶向治疗之一。”(西妥昔单抗是一种靶向EGFR的单克隆抗体,EGFR是本研究中发现的与STAT3相互作用的关键蛋白之一)。“我们希望这项研究将导致新的药物开发,并为口腔癌患者提供希望,特别是那些目前预后非常差的侵袭性口腔癌患者。”
 生物通微信公众号
生物通微信公众号
知名企业招聘